2021年3月2日、京都大学デジタルヘルスセミナー「SaMDを巡る動向と京都大学の新たな取組み」がオンラインで開催されました(1)。2020年は、医療機器プログラム(Software as a Medical Device、以下「SaMD」)に様々な観点で注目を集まりましたが、このSaMDを巡る規制改革や国際的な動向についての最新情報の紹介とともに、京都大学において始動しつつあるデジタルヘルスに関する2つの取組について本セミナーで公開されました。今回は本セミナーの内容をご紹介します。
セミナーの概要は以下の通りです。
- KAHSIプロジェクトの立上げについて
- 講演者:京都大学医学部附属病院医療情報企画部長/教授 黒田知宏 氏
- SaMD(プログラム医療機器)に関する規制改革の動き
- 講演者:医療コンサルタント/㈱メディヴァ 代表取締役 大石佳能子 氏
- 『治療用アプリ』の開発投資・産業育成を促進する海外政策 ~主に保険償還の観点から~
- 講演者:㈱日本総合研究所 リサーチ・コンサルティング部門 シニアマネージャー 川崎真規 氏
- デジタルヘルス産学共創の場(KUDHA)への誘い
- 京都大学オープンイノベーション機構プロジェクトクリエイティブ・マネージャー 庄境誠 氏
なぜKAHSIプロジェクトの立ち上げに至ったか?
2014年、薬事法から薬機法に改正以降、医療用途のソフトウェアが医療機器に該当(SaMD)することになり、いまだ開発において一部混乱が見られているという話題は以前の記事(2)でも取り上げたとおりですが、混乱の大きな原因は、規制の考え方と一般的なソフトウェア開発のカルチャーの方向性が大きなズレがあることにあります。すなわち、開発・評価・流通といういずれのステージにおいても、一般的なソフトウェアとSaMDではギャップがあり、そのギャップゆえに、ともすれば違法なソフトウェアが流通してしまったり、革新的ソフトウェアが実用化されにくいと黒田氏は述べています。京都大学にはSaMDとなりうる多くの研究成果があるものの、それらがうまく社会に出せないというジレンマがありました。
このギャップにより生じる混乱を解決すべく、SaMD/non SaMDにかかわらず医療ソフトウェアの市販化へのインキュベーターとして立ち上げられたのがKAHSIプロジェクト(Kyoto Advanced Health Software Initiatives、KAHSI)です。SaMDにしろ、non SaMDにしろ、薬機法という制度がある以上、適切な形で社会実装していくことが必要であり、その社会実装までの道筋を示し、時には伴走することで、研究者やプログラマが安心して医療ソフトウェアを開発でき、また医療者や市民が安心して医療ソフトウェアを活用できるという流通基盤を構築し、京都大学を医療ソフトウェア開発のメッカとすることがKAHSIの目指す将来像です。
IoT技術の進展や個別化医療の実現により、日常生活と医療の境目が曖昧になってきており、「病院を社会に『埋め込む』(Embed Hospital into Our Daily Life)」という世界が現実味を帯びてきています。セミナーの中で、黒田氏はこれを「ソーシャルホスピタル」と形容しましたが、今後データ駆動型社会となっていくだろう中で、SaMDは医療におけるその中核を担うものとなるでしょう。そのような社会を構築するためのサポートをKAHSIが担うことが期待されます。
規制改革推進会議から見たSaMD関連制度の動向
続いて、大石氏から、令和2年から続く規制改革推進会議の動向とその中でなぜSaMDをトピックとして取り上げたのかという説明がなされました。大石氏は、規制改革推進会議で議論すべきトピックを選定する上で、「医療介護分野における規制の課題とは何か?」を定義することからまず始め、「法律・規則によって定められているもの」「自治体等のローカルルール」「診療報酬、介護報酬」「規定等の不存在、不明瞭、不徹底」を規制の課題と定義し、SaMDはその規制課題を複合的にあわせもった一つの大きな柱として取り上げたといいます。これまでの開催でSaMDに関連する会合は3回おこなわれています。(どのような議論がなされたかについては、以前の記事(2)(3)(4)でもとりあげておりますので、ご覧ください。)
規制改革推進会議で議題としてとりあげられたことから、厚生労働省はDaSH for SaMDというSaMD開発促進パッケージ戦略(5)を打ち出し、制度設計に向けて動き始めています。しかしながら、厚生労働省はコロナ関連政策を始めとして大きな課題を数多く抱える省であり、またパッケージ戦略の詳細がこれから議論が始まる段階であることから、規制改革推進会議としては期限の設定やスケジュールに基づいたリソースの確保などがしっかりと行われているかをフォローしていく必要があるとのことでした。
河野行革担当大臣も言及するようにSaMD大国になりえるポテンシャルのある日本が、規制を含めて今の社会の枠組の中でそれを実現しづらいという課題に対して、規制改革推進会議の働き方が期待されます。
SaMD保険戦略の何が課題なのか?
続いて、3人目の演者である川崎氏からは、我が国におけるSaMDの保険償還に関する議論の動向紹介やSaMDの一種である治療に用いるアプリの海外での保険償還方法について詳細な説明がされました。本講演の中で、特に「治療用アプリ」と言われる患者と医療従事者が使用する治療用SaMDに関して薬事承認においても保険償還においても海外の制度は参考になるのではないかと紹介しています。
日本においても2020年にようやっと初の治療用アプリが薬事承認・保険償還されましたが、すでに海外では多くの治療用アプリが社会実装されています。例えば、米国では2010年の段階で糖尿病治療用アプリ(WellDoc社)がアメリカ食品医薬品局FDAにより認可され、他にも、喘息/慢性閉塞性肺疾患(COPD)患者向け治療用アプリ(Propeller Health社)など様々な疾患領域での治療用アプリが出現しています。
日本においても、この動きは加速していくものと期待されているものの、世界に追いつきそしてリードする産業としていくためには、治療効果や価値の高い治療用アプリを患者に提供するために、安全性やセキュリティ等の確保を前提にではありますが、 治療用アプリの保険償還において、①開発促進、②改良促進による産業育成を図るべきであると川崎氏は述べています。
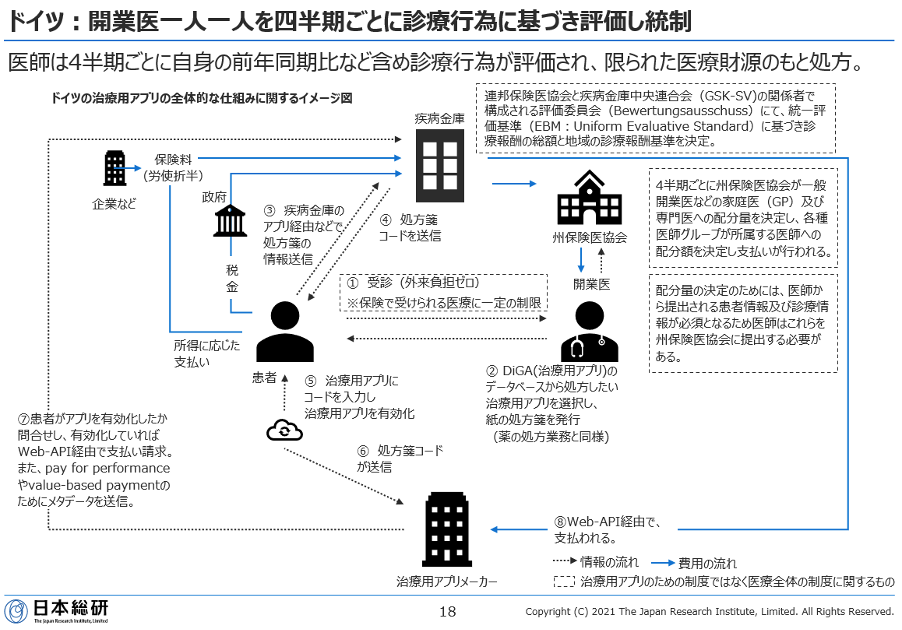
開発促進の観点で、参考となりうる制度をもつ国がドイツです。ドイツはデジタルヘルスケア法(Digitale-Versorgung-Gesetz – DGV)というデジタルおよびイノベーションによる医療発展を促す法律が制定され、たとえば治療用アプリ(Digitale Gesundheitsanwendung – DiGA)の処方権などが記載されました。そして、治療に貢献するアプリに特化した薬事承認・保険償還制度(DiGA Fast Track)を2019年12月より新たに運用しています。この1年半の中ですでに、薬事登録済のアプリが4件、薬事仮登録のアプリが7件あり、開発促進に寄与していると言えるでしょう。また、この政策の中で特徴的な点のひとつは、臨床評価に後ろ向き(レトロスペクティブ)の臨床研究(臨床試験でなくても良い)を活用可能としていることです。保健省内のシンクタンクであるHIH(Health Innovation Hub)のJan Broenneke氏はYouTubeで、「我々は治療用アプリにおいてRCTをゴールデンスタンダードと捉えていない。リアルワールドデータ(RWD)などレトロスペクティブ研究がスタンダードである。」と話しています。これは、従来の薬事承認審査においては、世界的に前向きの評価が必要とされることが主流ですが、治療用アプリにおいては前向きの評価をすることで社会実装が遅れてしまい、アプリの利点である開発スピードを疎外してしまうということが懸念されるためと推測されます。
さらに、これらのアプリに対して、ドイツでは1年目から保険償還価格が設定されます。1年目は仮償還となりますが、製造業協会と疾病金庫中央連合会(National Association of Statutory Health Insurance Funds:GSK-SV)がメーカー設定価格の上限を決定し、それに基づき、メーカー自らで保険償還価格を設定することができます。また、2年目以降の保険償還価格についても、製造業協会とGSK-SVが2年目以降の価格幅を決定しており、その価格幅を元にメーカーがGSK-SVと価格交渉することで2年目以降の価格が決定されます。また、1年目は2年目よりは安い最高価格を設定する必要があります。これらのシステムは、開発メーカーにとって保険償還価格に対する予見性が高く、開発の出口戦略という観点で大変有用であると言えます。
しかし、今後もしドイツで多くのアプリの薬事登録が進む場合、これらのアプリを使用する患者が増加するほど、医療財源に影響を与える可能性が懸念されますが、ドイツではこれに対してどのような対策を打っているのでしょうか?
実は、ドイツの保険制度において、医師は4半期ごとに自身の前年同期比などを含め診療行為が評価され、医療配分が統制されているというシステムとなっています。国の連邦保険医協会とGSK-SVの関係者で構成される評価委員会(Bewertungsausschuss)が、 統一評価基準(EBM:Uniform Evaluative Standard)に基づき診療報酬の総額と地域の診療報酬基準をまず決定します。それを受けて、各州の保険医協会が4半期ごとに一般開業医などの家庭医(GP)及び専門医への配分量を決定し、各種医師グループが所属する医師への配分額を決定し支払いが行われます。この配分料の決定のためには、医師から提出される診療患者情報及び診療情報が必須となるため、医師はこれらを州保険医協会に提出する必要があります。 治療用アプリもこの枠組の中で採用されるため、のべつ幕なしに利用されるわけではないということになります。海外の医療制度を日本へそのまま適用せよということではありませんが、このように、医療費統制の仕組みを備えた上での、治療用アプリの保険償還設定ポイントの前倒しは、今後日本における治療用アプリの保険収載方法を検討する上で参考となる手法かもしれません。
次に、改良促進の観点においてですが、薬事の観点ではプログラムの機能更新への対応を目指すIDATEN制度や、保険償還の観点においては学会を通した医療技術再評価提案書、チャレンジ申請といった制度はすでに存在します。しかしながら、プログラム製品のアップデート頻度や内容に最適化された制度というものを今後考えていくのであれば、よりスピード感のある対応が可能な制度を構築することが更なる理想と言えます。すなわち、保険適用後の治療用アプリについて、「有効性がポジティブでないもの」を可視化・公表し、 診療ガイドライン、価格改定に反映する仕組みを取り入れ、自然とより有効性の高い治療用アプリが使われている環境が理想的である、と川崎氏は述べています。
現在、海外においては、英国をはじめとした複数の国でRWDを活用した医療技術評価(HTA)を採用しています。特に中国は活発にRWD政策を整備しており、国家主導で医療健康ビッグデータ区域センターをおくなど、RWD研究におけるハードとソフトの環境改善と実施推進が始まっており、これに呼応する形でRWD関連の対策強化に乗り出す製薬メーカーが増加しています。
日本においてもRWDを活用した市販後調査については、まずは医薬品で始まったところですが、治療用アプリはその性質から、RWDでの保険償還価格改定の仕組みを試すに適した製品とも言えます。そして、治療用アプリのRWDでの保険償還価格改定を議論するにあたり、治療回数評価だけではない『価値に基づく医療の実装』や、多数・多様な治療用アプリを処方しても 患者・医師の実務が煩雑にならないための治療用アプリの『データ連携・標準化』といった検討が必要になってくるのではないか、というのが川崎氏の見解でした。
なお、2021年3月24日に開催された中医協において、医療機器プログラムの保険償還方法について、今後本格的に議論していくということが示されました(6)。すでにある医療機器の保険償還制度から、どのように議論が進んでいくのかはまだ未知数ですが、海外での取組で参考になる部分があるのであれば積極的にトピックとして取り上げて欲しいと願うばかりです。
総合大学である京都大学にKUDHAを新設する意味
最後の講演は、京都大学オープンイノベーション機構の庄境氏より、京都大学のもうひとつの新たな取組であるKUDHAが紹介されました。総合大学である京都大学では、ヘルスケア全般における課題を、自然科学(工学、情報学、理学、農学、医学、薬学等)や社会科学(文学、法学、 経済学、社会学等)での研究成果を基に、デジタルテクノロジーで解決しようとする研究が広く行われています。しかしながら、研究者側は「研究をいかに展開し、社会実装すべきか良くわからない(開発資金調達や法律関係)」という悩みを持ち、一方で、企業側は「有望な研究者、 研究シーズとつながるための良い仕組みがない」という悩みをもっています。
その中で、研究者を守り、研究を育てるために立ち上げられたのが 「京都大学デジタルヘルス社会実装アソシエーション」(Kyoto University Digital Health Association、「KUDHA」)になります。コンソーシアムではなく、デジタルヘルスのアカデミア研究シーズを社会実装に運ぶ産学連携共創の場 (エコシステム) としていくことを目標とした取組であり、多くのステークホルダーの参画を広く募集しています。
京都大学をデジタルヘルスのメッカへ!
京都大学は多くの研究者を抱える国内屈指の大学であり、デジタルヘルスに繋がる多くの技術要素研究や臨床研究が進んでいます。その中で、大学が研究シーズをいかに社会に出していくのかという観点でKAHSI、KUDHAといった積極的な取り組みを打ち出し、研究者を後押ししていくシステムが構築されており、京都大学をデジタルヘルスのメッカとしていくのだというご関係者の強い思いが伝わってくるセミナーでした。
KAHSI、KUDHAについてご興味のある方はKAHSIの窓口からお問い合わせください。
講演者紹介
本セミナーの講演者の皆様のご経歴は下記の通りです。
黒田 知宏 氏
京都大学医学部附属病院医療情報企画部長/教授
京都大学工学部情報工学科卒業後、奈良先端科学技術大学院大学情報科学研究科助手、京都大学医学部附属病院講師、同医療情報部副部長(兼任)を経て、2007年大阪大学大学院基礎工学研究科准教授。2009年京都大学医学部附属病院准教授、13年京都大学医学部附属病院教授、同医療情報企画部長(兼任)、同病院長補佐(兼任)、同情報学研究科教授(兼担)、現在に至る。仮想・強調現実感、福祉情報学、医療情報学、ウェアラブル・コンピューティング等の研究に従事。日本ME学会阿部賞等受賞。IEEE、電子情報通信学会、生体医工学会学会、医療情報学会等の会員。博士(工学)。
大石 佳能子 氏
コンサルタント・事業家/㈱メディヴァ 代表取締役
大阪大学法学部卒、ハーバードビジネススクールMBA終了後、マッキンゼーアンドカンパニー(米国)に入社。32歳でパートナー(役員)に就任。第一子を出産時に病院や医師の対応に違和感を感じ、「患者視点での医療改革」を目指して、Medical Innovation and Value-addedを意味する株式会社メディヴァ(MEDIVA)を設立。現在、資生堂、参天製薬、江崎グリコ等の非常勤取締役。内閣府規制改革推進会議医療介護WG座長、大阪大学経営協議会委員等を務める。
川崎 真規 氏
㈱日本総合研究所 リサーチ・コンサルティング部門 シニアマネージャー
関西大学総合情報学部卒業。高校まで、NHK「中学生日記」出演など子役として活動、IT企業、外資系コンサルティングファームを経て、(株)日本総合研究所に入社。2009年に中国医療戦略コンサルティング事業を立上げ、日綜(上海)北京諮詢分公司副総経理として現地に赴任。10年間、北京・上海を中心に現地日系医療企業へ常駐し戦略コンサルティングおよび中国医療政策研究に従事。2019年4月に帰任し、現在は、議員・官公庁・企業・アカデミアなどと日本の医療政策課題の研究・提言にも従事。
庄境 誠 氏
京都大学オープンイノベーション機構 プロジェクトクリエイティブ・マネージャー
京都大学工学研究科数理工学専攻前期博士課程修了後、旭化成工業(現旭化成)に入社。音声認識を始めとする、IT、IoT、AIなどの情報学分野の研究開発、事業化に一貫して従事。情報技術研究所所長、グループフェローに就任。海外からの技術導入、クラスII医療機器認証取得及び国内臨床研究の経験も持つ。奈良先端科学技術大学院大学情報科学研究科に社会人学生として入学。博士(工学)。2019年6月より、京都大学オープンイノベーション機構に移る。「組織」対「組織」の大型産学連携共同研究の組成・マネージメント及び社会実装の方法論の研究・開発に興味を持つ。
参考文献
(1)京大オリジナル株式会社:京都大学デジタルヘルスセミナー「SaMD(プログラム医療機器)を巡る動向と京都大学の新たな取組み」
(2)Digital Health Times:規制改革推進会議で取り上げられた医療機器プログラム(SaMD)の開発促進における課題-前編-
(3)Digital Health Times:規制改革推進会議で取り上げられた医療機器プログラム(SaMD)の開発促進における課題-後編-
(4)Digital Health Times:デジタルヘルスに残された議論〜規制改革推進会議でのやりとり〜
(5)厚生労働省:プログラム等の最先端医療機器の審査抜本改革
(6)厚生労働省:中央社会保険医療協議会 総会(第477回) 議事次第
