昨年の秋頃に、SaMDの開発促進を盛り上げていくために活動をしている業界団体として、JaDHAをご紹介する記事(1)を公開しました。時間がかなり空いてしまいましたが、今回は国内の医療機器産業業界団体として最大手である一般社団法人 日本医療機器産業連合会(通称、「医機連」) (2)についてご紹介します。
医機連とは
医機連とは、1984年(昭和59年)に旧名称である日本医療機器関係団体協議会として、医療機器、医療材料等の開発、生産、流通に携わる医療機器関係団体の参加により設立された業界団体です。医療機器は多種多様であることから、そのタイプごとに様々な業界団体が存在(例:電子情報技術産業協会、日本医療機器工業会、など)しており、これらの各医療機器関係団体の主体性を尊重しつつ、内外の共通問題等についての調査・研究を行い、その対策を講じ、業界の公正な意見をとりまとめ提言を行う等、業界の発展と国民の健康福祉の増進に寄与しています。
医機連は、医療機器・医療技術のイノベーションと安定供給を通じて、日本をはじめとして世界に優れた医療機器テクノロジーを提供し、もって国民福祉の向上と医療機器産業の発展に寄与することを目指しています。2023年6月時点で正会員として20の業界団体が参加しており、また多くの個別企業が賛助会員として参加しています。
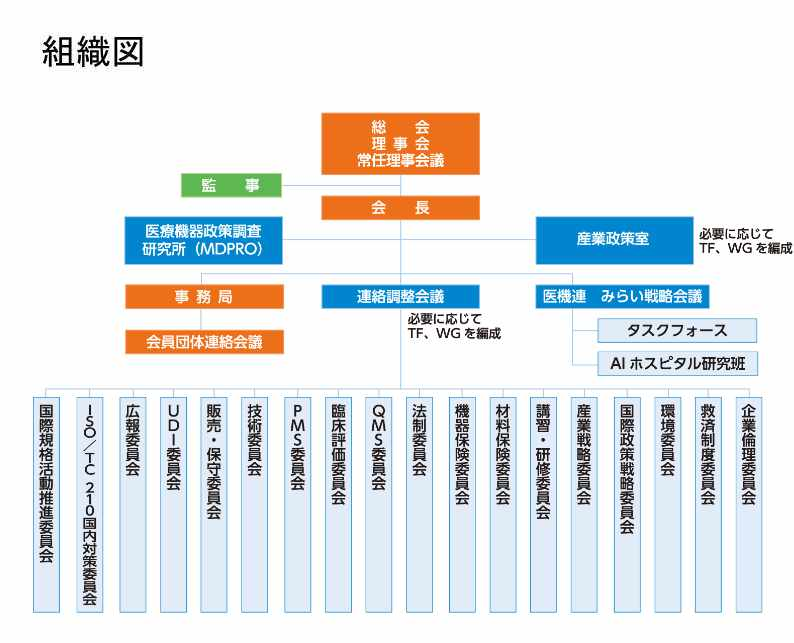
医療機器には様々な切り口での課題が存在することから、医機連には多くの常設委員会が存在し、会員の団体から選出されたメンバーが委員会で活動しています。
プログラム医療機器対応WGとは
これら常設の委員会に限らず、臨時で対応が必要なトピックについては、別途ワーキンググループ(以下、「WG」)が立ち上がることもあり、近年活発に活動しているWGの一つとして「プログラム医療機器WG」があります。
2014年の法改正により新しいカテゴリーとして誕生した「プログラム医療機器」については、これまでの記事でもご紹介してきた通り、従来の有体物の医療機器とは異なる特性があることや新しい領域の製品であるがゆえにこれまでとは異なる開発のハードルがあります。特にこの領域は新規参入企業が多く、医機連に所属していない企業も多々あるものの、医療機器の業界団体としてワンボイスで確認作業や要望をまとめていくことが望ましいという観点から、医機連が中心的な役割を担う「プログラム医療機器対応WG」が2021年に立ち上がりました。
したがって、このWGの目的は、医療機器産業の立場でプログラム医療機器に関連する政策の在り方を規制の観点、診療報酬の観点、産業振興の観点などから総合的に検討し、必要に応じて提言を行うといえるでしょう。
プログラム医療機器対応WGの活動
プログラム医療機器対応WGでは、規制対応sub-WGと保険対応sub-WGという2つのsub-WGに分かれて議論が進められています。参加メンバーは医機連傘下の業界団体から選出された委員を中心とし、それ以外にも一般社団法人米国医療機器・IVD工業会(通称、「AMDD」)(3)、欧州ビジネス協会(通称「EBC」)(4)といった外資系医療機器メーカーの業界団体からの代表者、そしてスタートアップ企業からの有識者も参加しています。
規制対応sub-WGの役割
プログラム医療機器の規制に関する課題整理を行っています。具体的には、プログラムの医療機器該当性判断に関する課題やプログラム医療機器の規格に関する課題、承認審査に関する課題など多岐に渡ります。
特に、開発の入り口にあたる該当性判断については、多くの企業が躓くポイントでもあり、厚生労働省の担当部署と意見交換をしながら、該当性ガイドラインの解説書の作成(5)や講演会の開催(6)などをこれまでに行ってきています。
これらの課題を整理しながら、より良いルールメイキングを進めていくために民間側から行政との対話を行っています。
保険対応sub-WGの役割
医療機器を開発する上での出口問題として、保険上の評価がどのようになされるのかという問題があります。(開発したらどのくらいの値段で販売ができるのかがわからなければ、開発に着手することが難しいという企業がいることは想像に難くありません。)
プログラム医療機器は、まだ製品数が限られており、保険償還されている製品はさらに事例が限られることから、保険上の評価がより明確にしてほしいといった要望が各所から出ており、医機連の保険対応sub-WGではどのように評価をしてほしいかという要望をまとめ、行政との意見交換を行っています。

今後の活動について
昨年の10月に開催された内閣府規制改革推進会議(7)では、医機連が医療機器産業の代表団体として意見陳述(8)を行っています。この会議では、医機連だけでなく、以前の記事でご紹介したJaDHAやヘルスケア系ベンチャー企業の業界団体である日本医療ベンチャー協会も意見陳述を行っており、この会議をきっかけとしてこの半年で様々な議論が進んでいます。(これについては次回の記事でご紹介させてください。)
医機連のプログラム医療機器対応WGの活動は、今年度も継続して活動が予定されています。新技術の開発や質問自体のスピードが早まっている中、SaMDはその影響を大きく受けることが想定され、これまでの課題だけでなく、新たな課題も出てくることでしょう。それらの課題をいかに拾い上げ、行政に建設的な提案ができるのか、業界団体としての手腕がこれからも問われます。
参考資料
(1)Digital Health Times:SaMD開発促進のために活動する業界団体の動向(1)
(4)欧州ビジネス協会
(5)一般社団法人 日本医療機器産業連合会:プログラムの医療機器該当性ガイドラインに関する解説書_医機連編_第1.0版_2022.10.20
(6)一般社団法人 日本医療機器産業連合会:『2021/12/10開催_プログラム医療機器に関する質疑応答会』質疑と回答メモの公開
(7)内閣府規制改革推進会議:第1回 医療・介護・感染症対策ワーキング・グループ 議事次第
(8)内閣府規制改革推進会議:資料2-3一般社団法人日本医療機器産業連合会 御提出資料(PDF形式:1,452KB)
